
第一节 FISH技术的基本原理及优势
荧光原位杂交(fluorescenceinsituhybridization,FISH)是近些年较为常用的分子细胞遗传学技术、该技术通过已知的核苷酸片段与靶DNA形成靶DNA与核酸探针的杂交体,可直接在组织切片(冷冻切片或石蜡切片)、细胞涂片、染色体制备标本或培养细胞爬片上杂交。该技术操作简单、快速、直观、灵敏度高,目前广泛应用于医学研究及某些遗传疾病和肿瘤的临床诊断。
一、原理
FISH是以荧光素标记已知序列的核苷酸片段(探针)与荧光素标记的特异亲和素之间的免疫化学反应,经荧光检测体系在显微镜下对待测DNA进行定性、定量或相对定位分析。具有敏感、快速、能同时显示多种颜色等优点,不但能显示中期核分裂象的染色体,还能检测间期细胞核的DNA。
二、优势
自20世纪80年代末,Pinkel和Heiles将FISH技术引入染色体检测领域后,FISH技术就在临床诊断及科研工作中得到了广泛的运用,显示出与一些传统技术相比的明显优势。与传统的免疫组织化学法(IHC)相比,FISH技术具有良好的稳定性和可重复性。此外,荧光原位杂交结果的判定借助于对荧光的颜色判断和信号计数,客观地量化了检测结果。FISH的另一个特点是可以联合应用多种标记系统,在一次杂交中可检测多种探针在染色体上的位置及探针间的相互关系,即多色FISH或多靶FISH。与其他分子生物学检测手段相比,FISH可以在组织和细胞结构相对完整的前提下,在癌细胞原位分析单细胞核内基因的变化,同时又排除了其他非癌细胞的干扰,所以已广泛应用于肿瘤研究中的基因扩增、易位重排及缺失等的检测,在肿瘤诊断和鉴别诊断、预后和治疗监控等方面都有重要意义。
第二节 荧光原位杂交的实验操作
一、探针标记
FISH探针一般采用随机引物法或切口翻译法,如将PCR技术引入FISH探针标记,可使其灵敏度提高到0.25kb。应用TSA系统(tyramidesignalamplification)能将杂交信号再放大1000倍,可用于单拷贝基因的定位。FISH分辨率大约为1~3Mb,如果应用强变性剂处理染色体,让DNA分子从蛋白质中分离出来,使双DNA完全伸展并黏附在玻片上,经预处理后,分辨率可达1~2kb。还可采用对分裂中期染色体进行显微解剖(microdissect)法以提高分辨率。
探针的荧光素标记可以采用直接和间接标记的方法。间接标记是采用生物素标记DNA探针,杂交之后用耦联有荧光素亲和素或链霉亲和素进行检测,同时利用亲和素-生物素-荧光素复合物,将荧光信号放大,从而可以检测500bP的片段。直接标记法是将荧光素直接与探针核苷酸或磷酸戊糖骨架共价结合,或在缺口平移法标记探针时将荧光素核苷三磷酸掺入。
由于间接法的操作步骤较为繁琐,所以目前直接法的使用更为广泛。
二、实验相关设备
1.荧光原位杂交成像系统(图20-2-1),包括荧光显微镜及相应的滤光片组、分析软件。
2.42℃恒温孵箱或杂交仪(图20-2-2),立式染缸(考普林瓶)、计时器、水银温度计。
3.恒温水浴箱、旋涡混合器、离心机、烤片机、移液器。
4.pH计或精密pH试纸、载玻片、盖玻片、0.5ml离心管。


图20-2-1荧光原位杂交成像系统 图20-2-2杂交仪
三、实验操作
荧光原位杂交技术总体上分为:预处理阶段,变性杂交阶段,玻片后洗阶段,复染阶段,镜检结果阶段。检测试剂盒应该使用国家食品药品监督管理局(SFDA)认可的产品。
不同公司生产的探针试验方法略有不同,由于采用不同的探针试剂,诊断技术操作方法会有差异,所以本文以Her-2探针为例,讲解其实验步骤,各实验室要开展荧光原位杂交技术应结合说明书进行操作,现介绍两种操作方法:
(一)操作步骤(以金菩佳试剂盒为例)
1.组织预处理
(1)组织经10%中性福尔马林固定,石蜡包埋,切片4~5μm,置于防脱载玻片上。
(2)将组织切片置于65℃烤箱内过夜。
(3)切片脱蜡至蒸馏水。
(4)30%酸性亚硫酸钠(sodiumbisulfite)50℃处理组织切片20~30min;或用90℃去离子7理组织切片20~30min。
(5)室温下于2×SSC溶液中漂洗2次,每次5min。若用90℃去离子水则省略此步骤。
(6)切片浸泡在蛋白酶K工作液(终浓度200μg/ml)中,37℃孵育5~30min。
(7)切片经蛋白酶K消化后,于2×SSC溶液中漂洗2次,每次5min。
(8)室温下将切片依次置于70%乙醇、85%乙醇和无水乙醇中各2min脱水。
(9)自然干燥切片。
2.变性杂交
(1)荧光原位杂交有杂交仪变性杂交和甲酰胺变性杂交两种方法。前者是用杂交仪对样本和探针进行共变性,减少人为因素的影响;后者是样本和探针分别进行变性。
(2)杂交仪变性杂交(自动操作):设置杂交仪器共变性条件:83℃5min,杂交条件:42℃,16~18h(不同公司探针请参考说明书)。
将探针(2.0μl)、杂交缓冲液(7.0μl)和去离子水(1.0μl)加入EP管(依据试剂说明书推荐使用),涡旋混匀后短暂离心1~3s,滴加于切片杂交区域,加盖盖玻片,用橡皮胶封边,避免产生气泡。放入杂交仪中杂交。
3.杂交后洗涤
(1)将切片置于室温50%甲酰胺/2×SSC溶液中移去盖玻片。
(2)将切片置于(46±1)℃50%甲酰胺/2×SSC溶液中,漂洗5min×3次。
(3)将切片置于(46±1)℃2×SSC溶液漂洗4min。
(4)将切片置于(46±1)℃0.1%NP-40/2×SSC中,漂洗5min。
(5)将切片置于2×SSC5s后迅速将其置于70%乙醇中,漂洗3min。
4.复染暗处自然干燥切片后,将15μlDAPI复染剂滴加于杂交区域,立即盖上盖玻片。放置10~20min后,在荧光显微镜下选用合适的滤光片组观察切片。
(二)操作步骤二:
现介绍Abbott公司的PathvysionHer-2DNAProbeKit的操作方法,预处理的试剂盒为Abbott公司的VysisPareffinPretreatmentReagentkit。
1.组织杂交前处理
(1)组织经10%中性福尔马林固定包埋,切片4~5μm,置于防脱载玻片上烤片60℃过夜。
(2)切片脱蜡至蒸馏水。
(3)预处理液(pretreatmentsolusion)80℃处理切片10min后蒸馏水洗3min,室温空气中干燥2~5min。
(4)放入37℃水浴预热的消化液(proteasebuffer+pepsion)中孵育10~60min后蒸馏水洗3min,室温空气中干燥2~5min。
(5)将切片梯度脱水,空气中干燥。
2.变性杂交加适量探针于组织上盖玻片封片,用橡皮胶封片放入杂交仪中杂交过夜。设置杂交仪器共变性条件:75℃5min,杂交条件:37℃,16~18h。
3.杂交后洗涤
(1)从杂交仪中取出昨日玻片,去掉封片胶。
(2)准备两缸washbuffer备用,在第一缸洗脱液(washbuffer)中去掉盖玻片。
(3)74℃水浴预热的第二缸洗脱液(washbuffer)中漂洗2min。
(4)空气中干燥。
4.复染加适量DAPI复染剂于杂交区域,盖上盖玻片,置于荧光显微镜下观察。
四、镜检结果
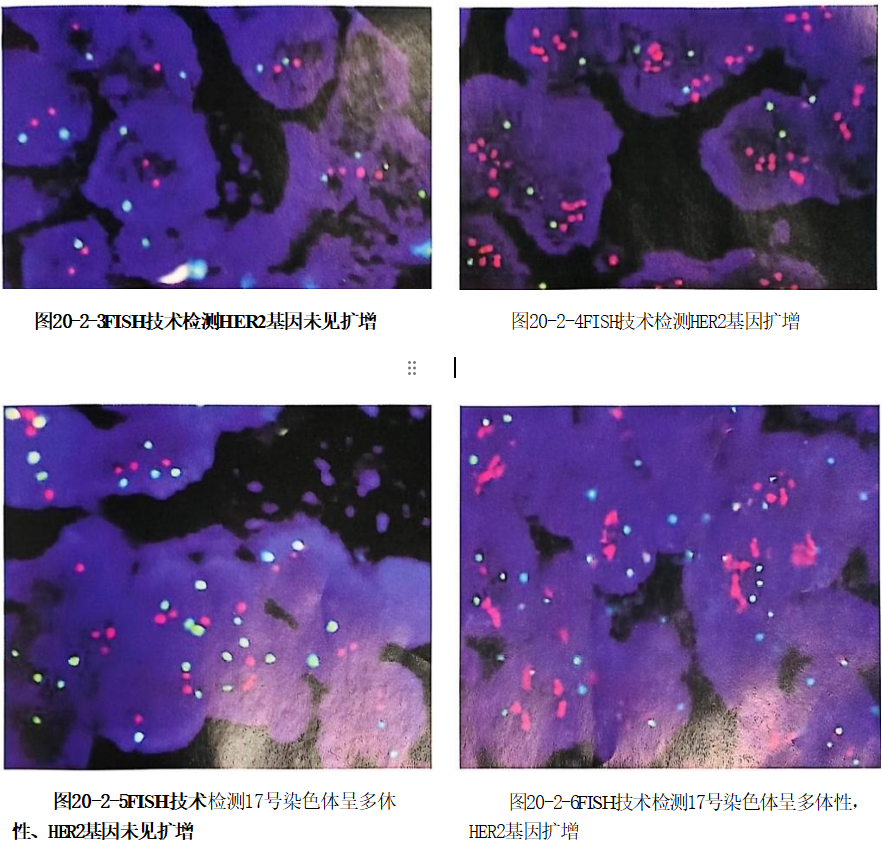
荧光显微镜观察,通过专用软件合成彩色图像,摄影保存FISH结果,进行结果判定(图20-2-3~20-2-6):
随机计数20个细胞,统计Ratio值(Ratio值=20个细胞核中红信号总数/20个细胞核中绿色信号总数):
Ratio<1.8为阴性结果,提示样本无Her-2基因扩增。
Ratio>2.2为阳性结果,提示样本存在Her-2基因扩增。
Ratio介于1.8~2.2之间时为临界值,可增加计数细胞至60~100个,或重做FISH实验来判断最终结果。
计数细胞必须是各通道信号均清晰可辨的细胞,细胞核轮廓不清或有重叠的不要分析。
杂交不均匀的区域不要分析。
背景深影响信号判断的区域不要分析。
在分析石蜡切片时,分析的区域应在肿瘤细胞集中的部位(需由病理科医师认定)。
如果超过25%的细胞核内信号太弱,则该区域不要进行分析。
如果超过10%的细胞质内有信号,则该区域不要进行分析
五、FISH检测操作注意事项
1.组织处理须标准化,应尽可能缩短取材到固定的时间。在观察完大体标本特征后,将组织每隔5~10mm呈书页状切开充分固定,组织固定液为10%中性福尔马林缓冲液,最佳固定时间6~48h。有的公司探针超过6周的石蜡切片不宜再用于Her-2检测,有的公司探针对几年或几十年的蜡块仍可用于Her-2检测。
2.实验程序必须标准化。任何检测结果的偏差均需报告,并重新进行确认调整。
3.实验室在每一轮检测中均应使用标准化对照材料(阳性、阴性)。
4.切片在后洗液中应严格掌握温度和时间,可降低背景。
5.杂交后的玻片应注意避光,尽量不要暴露于日光灯和阳光下,存放于避光玻片盒内。根据荧光染料的不同,选择相应的荧光显微镜滤色片。
6.荧光信号容易淬灭,染色后应及时在荧光显微镜下观察结果,同时摄影保存图像。如果当时不观察,可将切片放入-20℃避光的盒内保存,两个月或更长时间仍可保持良好。
7.试剂不宜反复冻融。
8.探针使用前应先混匀后离心,注意避光。
9.报告Her-2结果的医生应相对固定。
10.在乳腺癌Her-2结果判断时,应选择浸润性病变部位。
11.在进行细胞计数信号时,应至少2个人随机判读肿瘤细胞信号,至少计数20个细胞。